乳腺癌
發布時間:2023-03-21 09:59:47 人氣:1460
Adv. Sci. 2022:酸降解產氫MOF材料克服癌癥耐藥/轉移和脫靶副作用

背景
開發既能控制藥物釋放又具有高生物安全性的刺激響應性可降解多孔載體對其臨床轉化至關重要,但目前仍具有挑戰性。本文通過卟啉與零價鐵原子的配位,設計了一種新型的卟啉-鐵金屬有機骨架(Fe-MOF)納米晶體,作為酸降解的藥物載體和氫供體。Fe-MOF納米晶體表現出優異的酸響應降解能力,可以產生氫氣并同時釋放負載藥物,用于癌癥多藥耐藥(MDR)和轉移的氫聯合化療,以及局部氫消除藥物對正常細胞/組織的脫靶毒副作用。在機制上,釋放的H2通過免疫激活瘤內M1表型巨噬細胞,從而下調轉移相關基質金屬蛋白酶-2 (MMP-2)的表達,幫助化療藥物有效抑制腫瘤轉移,并下調MDR癌細胞中p -糖蛋白(P-gp)蛋白和三磷酸腺苷(ATP)的表達,使化療藥物增敏,增強對線粒體和DNA的損傷。高抗MDR/抗轉移性和高生物相容性使Fe-MOF納米晶體和基于Fe-MOF的納米藥物具有很高的臨床轉化潛力。
圖文導讀
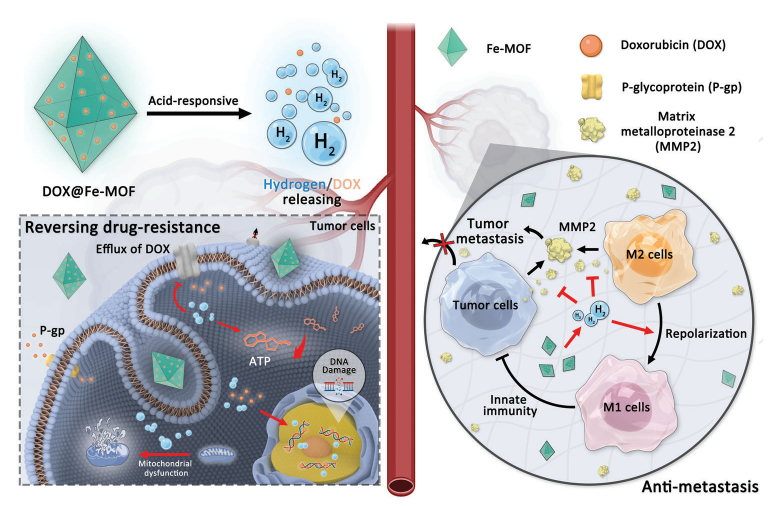
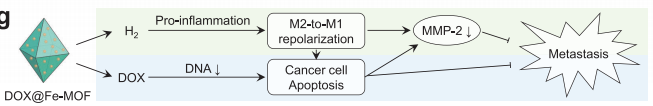
(圖1 從DOX@Fe-MOF納米晶體中釋放酸反應性氫/藥物以克服癌癥耐藥/轉移的示意圖)

(圖2 Fe-MOF納米晶的合成路線及形貌和結構)

(圖3 酸反應性降解和氫/藥物釋放譜)
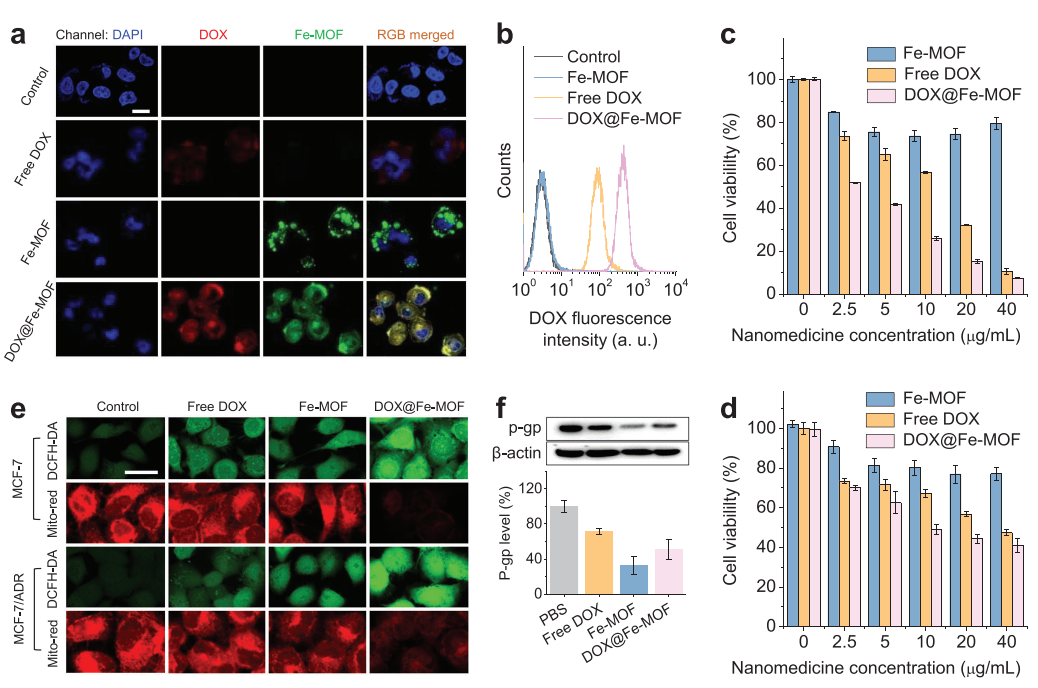
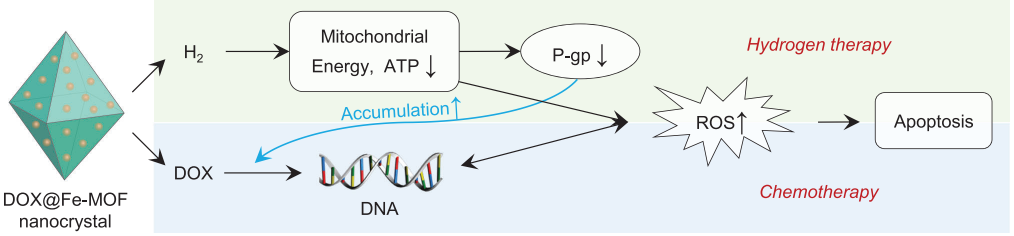
(圖4 體外氫聯合化療治療癌癥耐多藥的療效及機制研究)
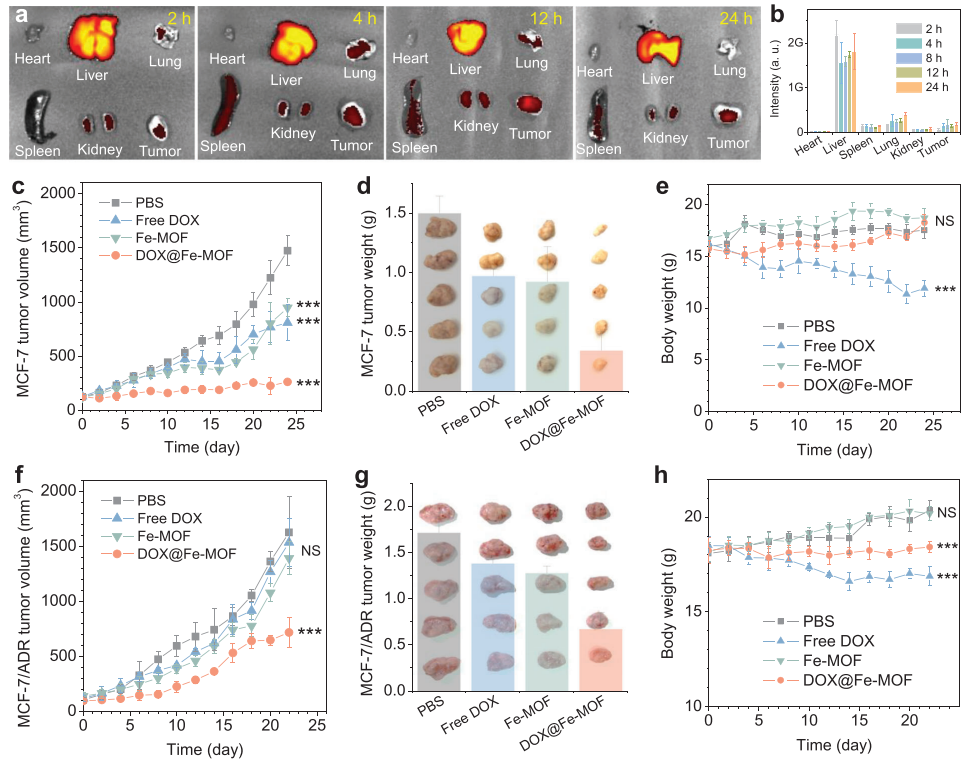
(圖5 體內氫聯合化療(n = 5個獨立實驗))

(圖6 DOX@Fe-MOF納米藥物對原發性乳腺腫瘤生長和肺轉移的抑制作用)
全文總結
開發了一種新型的Fe-MOF納米晶體作為耐多藥和轉移的氫聯合化療的藥物載體和氫供體。所構建的DOX@Fe-MOF納米藥物具有優異的酸響應降解和氫/藥物釋放行為。納米藥物釋放的氫氣通過下調P-gp表達和降低ATP水平,增強ROS介導的DNA損傷,有效增敏MCF-7/ADR細胞的化療,并通過免疫激活M1巨噬細胞和抑制MMP-2表達,輔助DOX有效抑制轉移。另一方面,納米藥物釋放的氫氣也減少了DOX對正常組織的毒副作用,使DOX@Fe-MOF納米藥物具有良好的生物相容性和生物安全性。高抗MDR和抗轉移效果和高生物安全性得益于DOX@FeMOF納米藥物優異的通用性Fe-MOF平臺,保證了其臨床轉化的高潛力。
原文鏈接:https://doi.org/10.1002/advs.202101965
僅用于學術分享,侵權請聯系刪除,歡迎交流。
| 溫馨提示:蘇州北科納米供應產品僅用于科研,不能用于人體,不同批次產品規格性能有差異。網站部分文獻案例圖片源自互聯網,圖片僅供參考,請以實物為主,如有侵權請聯系我們立即刪除。 |
上一篇: 軟骨缺損修復


