╚A¢|└Ē╣ż┤¾īWŅÖĮśŪĪČCMĪĘŻ║╝{├ūĮķ┐ūMOFs┐ūĄ└ā╚╝ē┬ō╔·╬’Ę┤æ¬Ų„Ą─Č©╬╗śŗĮ©╝░Ųõė├ė┌╝Ü░¹ā╚╗Ņąį觥─ŪÕ│²
░l▓╝ĢrķgŻ║2021-04-07 09:06:47 ╚╦ÜŌŻ║1866
╔·├³¾wā╚Ą─ģ^╩ę╗»║═╝ē┬ōĘ┤æ¬╩Ūūį╚╗ĮńųąīŹ¼F╝Ü░¹ā╚┤·ųx║═║═Ė▀ą¦ą┼ŽóĮ╗┴„Ą─╗∙▒ŠįŁätŻ¼įōĘNĘĮ╩Į─▄ē“į╩įSųąķg«a╬’į┌Ė„┤▀╗»å╬į¬ų«ķgĄ─Ė▀ą¦║═Č©Ž“▐DęŲĪŻę“┤╦Ż¼į┌╚╦╣żŽĄĮyųą─ŻöM▀@ĘNĖ▀ą¦ėąą“Ą─╝{├ū╬óŁhŠ│ę²Ų┴╦╚╦éāĄ─śO┤¾┼d╚żĪŻ─┐Ū░Ż¼╗∙ė┌ČÓ┐ū▓─┴ŽĄ─ČÓĘN╔·╬’Ę┤æ¬Ų„ęčĮø▒╗ķ_░l│÷üĒŻ¼▓óŲ┌┼╬īó▓╗═¼├ĖĄ─┤▀╗»ū„ė├Ė▀ą¦┼╝┬ōŲüĒĪŻĮī┘ėąÖC╣Ū╝▄Ż©MOFsŻ®Ė▀Č╚┐╔š{Ą─ĮYśŗ║═┐╔ūāĄ─ĮM│╔│╔Ęų╩╣Ųõ│╔×ķśŗĮ©┤╦ŅÉ╔·╬’Ę┤æ¬Ų„Ą─└ĒŽļ▓─┴ŽĪŻMOFsĄ─ā×ä▌▓╗āHį┌ė┌┐╔ęįī”Ųõ╬’└ĒĮYśŗ▀MąąįOėŗŻ¼ę²╚ļĮķ┐ūĮYśŗī”┤¾Ęųūė├Ė▀Mąąžō▌dŻ¼▀Ć┐╔ęįĖ─ūā┐ū▒┌╔ŽĄ─╗»īWĮM│╔Ż¼┘xėĶŲõ┐╔┼c├ĖŽÓģf═¼Ą─┤▀╗»ū„ė├ĪŻ╚╗Č°Ż¼į┌MOFsųą╩╣ė├▄ø─Ż░Õū„×ķĮYśŗī¦Ž“ä®ūįĮMčbą╬│╔Įķ┐ūĄ─═¼Ģr▒Ż│ųŲõĮYŠ¦ąį╚į╚╗╩Ūę╗éĆ╠¶æĪŻ▀@╩Ūė╔ė┌į┌MOFs╔·ķL▀^│╠ųąĮYŠ¦Ą─“īäė┴”═©│ŻĘŪ│ŻÅŖŻ¼ę“┤╦Ū░“ī¾wāAŽ“ė┌ā׎╚ĮYŠ¦Ż¼Č°īó─Ż░Õä®┼┼│²į┌ūįĮMčb▀^│╠ų«═ŌŻ¼╩╣Ųõ▓╗─▄ŲĄĮĮYśŗī¦Ž“Ą─ū„ė├ĪŻ
ßśī”╔Ž╩÷å¢Ņ}Ż¼╚A¢|└Ē╣ż┤¾īWŅÖĮśŪĮ╠╩┌łFĻĀį┌Ū░Ų┌蹊┐Ą─╗∙ĄA╔ŽŻ¼ķ_░l┴╦ę╗ĘNHofmeisterļxūėĮķī¦Ą─▄ø─Ż░ÕūįĮMčb▓▀┬įŻ¼īŹ¼F┴╦Įķ┐ūMOFsĄ─┐╔┐ž║Ž│╔Ż¼▓óį┌┤╦╗∙ĄA╔Žī”MOFsĄ─╬óĮķ┐ūĮYśŗ▀MąąĘų╝ē╣”─▄╗»Ż¼│╔╣”śŗĮ©┴╦╝{├ū╝ē┼╝┬ō╔·╬’Ę┤æ¬Ų„ė├ė┌╝Ü░¹ā╚╗Ņąį觥─ŪÕ│²ĪŻ╚ńłD1╦∙╩ŠŻ¼ū„š▀▓╔ė├UiO-66ą═MOFū„×ķ╗∙¾wŻ¼F127ū„×ķ─Ż░Õ䮯¼ClO4-ū„×ķ¹}╚▄ļxūėŻ¼║Ž│╔┴╦┐ūÅĮ╝s×ķ7 nmĄ─╝{├ūĮķ┐ūMOFsĪŻ═¼ĢrŻ¼Ą├ęµė┌Zr6łF┤ž┼õ╬╗ĘĮ╩ĮĄ─ČÓśėąįŻ¼Š▀ėą▀^č§╗»Üõ├ĖŻ©CATŻ®╗ŅąįĄ─Õi▀▓▀°Ęųūė┐╔ū„×ķ┼õ¾wę²╚ļĄĮ╣Ū╝▄ųąŻ¼┼cĮķ┐ūā╚žō▌dĄ─╠ņ╚╗│¼č§╗»╬’Ųń╗»├ĖŻ©SODŻ®ģf═¼ū„ė├śŗ│╔╝ē┬ō┐╣č§╗»ŽĄĮyė├ė┌╝Ü░¹ā╚╗Ņąį觯©ROSŻ®Ą─Ė▀ą¦ŪÕ│²ĪŻ
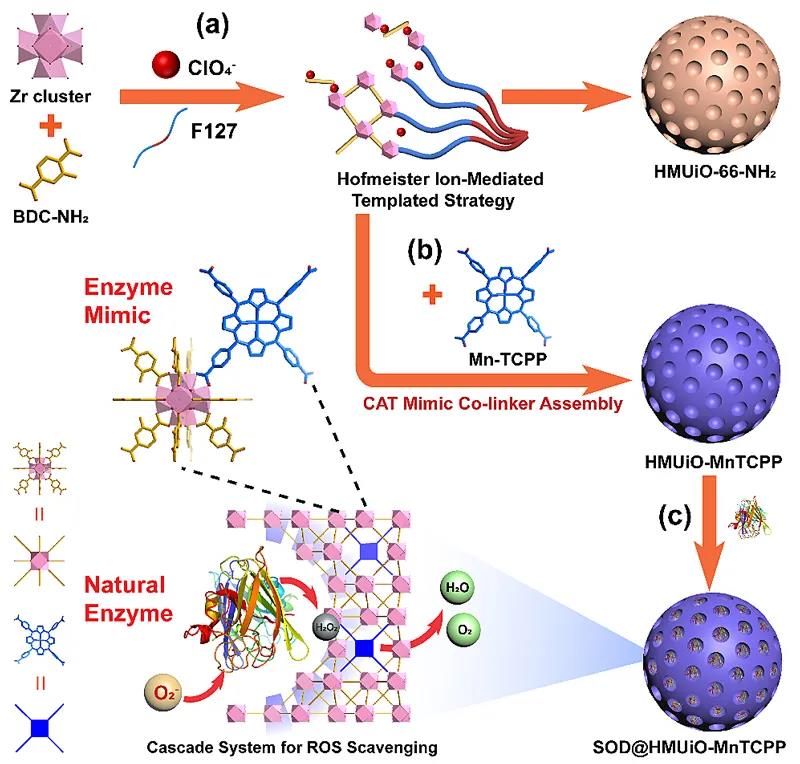
įō蹊┐łFĻĀ╩ūŽ╚═©▀^š{┐žĘ┤款wŽĄĄ─ģóöĄŻ¼Įę╩Š┴╦įōūįĮMčb▓▀┬įĄ─ų„ę¬ė░Ēæę“╦žĪŻ╩ūŽ╚Ż¼ū„×ķę╗ĘNHofmeister¹}╚▄ļxūėŻ¼ClO4-į┌▒Š¾wŽĄĮķ┐ūĄ─ą╬│╔▀^│╠Ųų°ĻPµIū„ė├ĪŻClO4-Ą─ū„ė├į┌ė┌į÷ÅŖMOFsŪ░“ī¾wė┌╣▓Š█╬’─z╩°ų«ķgĄ─ŽÓ╗źū„ė├Ż¼Å─Č°ūĶų╣ūįĮMčbŽĄĮyųą╣▓Š█╬’─z╩°║═MOFsŪ░“ī¾wĄ─ŽÓĘųļxĪŻį┌ø]ėąClO4-Ą─ŪķørŽ┬ų╗─▄½@Ą├ø]ėąĮķ┐ūĄ─UiO-66-NH2ĪŻŲõ┤╬Ż¼š{╣Ø䮥─ė├┴┐╩Ū┐žųŲ╝{├ūŅw┴ŻĮķ┐ūĮYśŗ║═ą╬├▓Ą─ĻPµIę“╦žĪŻę╗ŽĄ┴ąĄ─ī”ššīŹ“×▒Ē├„Ż¼«öš{╣Ø䮥─┴┐▌^╔┘ĢrŻ¼╦∙½@Ą├Ą─╝{├ū┴Żūė▌^ąĪŻ¼Ą½╩Ū«a╬’Ą─ĮYŠ¦Č╚▌^Ą═ĪŻ«öš{╣Ø䮥─╝ė╚ļ┴┐▀^ČÓŻ¼Ņw┴Żą╬ĀŅīóūāĄ├▓╗ęÄätŻ¼Ūę│▀┤ńį÷┤¾Ż¼▓╗└¹ė┌║¾└mīŹ“×ųą╝Ü░¹Ą─ā╚═╠ĪŻ
ū„š▀╩╣ė├Æ▀├ĶļŖńRĪó═Ė╔õļŖńRĪóĄ¬ÜŌ╬³ĖĮ£yįć║═Æ▀├Ķ═Ė╔õļŖūė’@╬óńRĄ╚╩ųČ╬ī”▓─┴Ž▀Mąą┴╦įö╝ÜĄ─▒Ēš„ĪŻĮY╣¹▒Ē├„įō▓─┴ŽĮķ┐ū│▀┤ń╝s×ķ7.4 nmŻ¼┴ŻÅĮ╝s100 nmŻ©łD2Ż®Ż¼Ūęį┌ōĮļs▀▓▀°┼õ¾wų«║¾ą╬├▓╝░ĮYśŗø]ėą░l╔·├„’@Ą─ūā╗»Ż©łD3Ż®ĪŻ
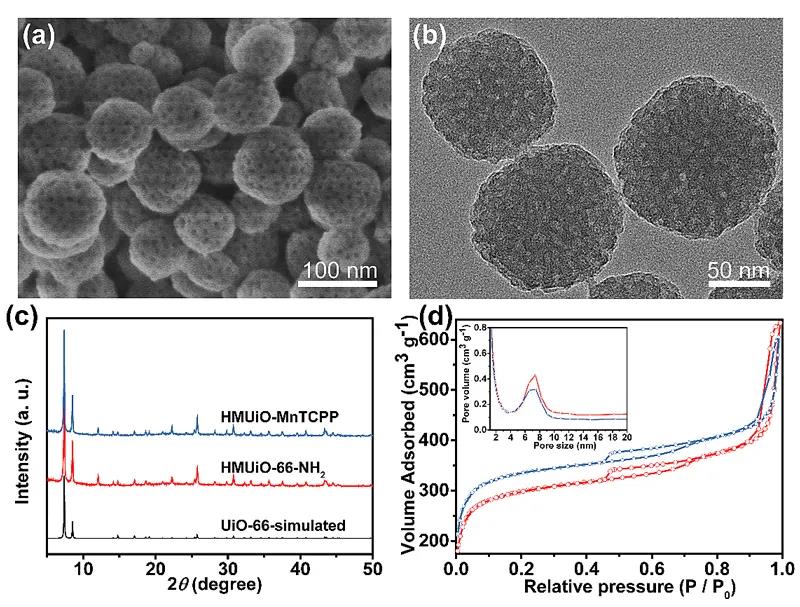

¾w═ŌīŹ“×ĮY╣¹▒Ē├„įōĮķ┐ūMOFsū„×ķ▌d¾w┐╔ī”žō▌dĄ─SOD╠ß╣®┴╝║├Ą─▒Żūoū„ė├ĪŻį┌ŠÅø_ę║ųąĮ■┼▌ę╗Č╬Ģrķg║¾Ż¼ŽÓ▒╚ė┌ė╬ļxĄ─SODŻ¼SOD@HMUiO-MnTCPP╚į╚╗Š▀ėą▌^Ė▀Ą─O2-ęųųŲ╗ŅąįŻ©łD4aŻ¼bŻ®ĪŻ═¼ĢrŻ¼ōĮļsĄ─Mn-TCPP┼õ¾w┘xėĶ┴╦HMUiO-MnTCPPŅÉCAT╗ŅąįŻ¼┐╔īóSOD┤▀╗»O2-«a╔·Ą─H2O2▀Mę╗▓ĮĘųĮŌ×ķH2O║═O2Ż©łD4cŻ¼dŻ®ĪŻ
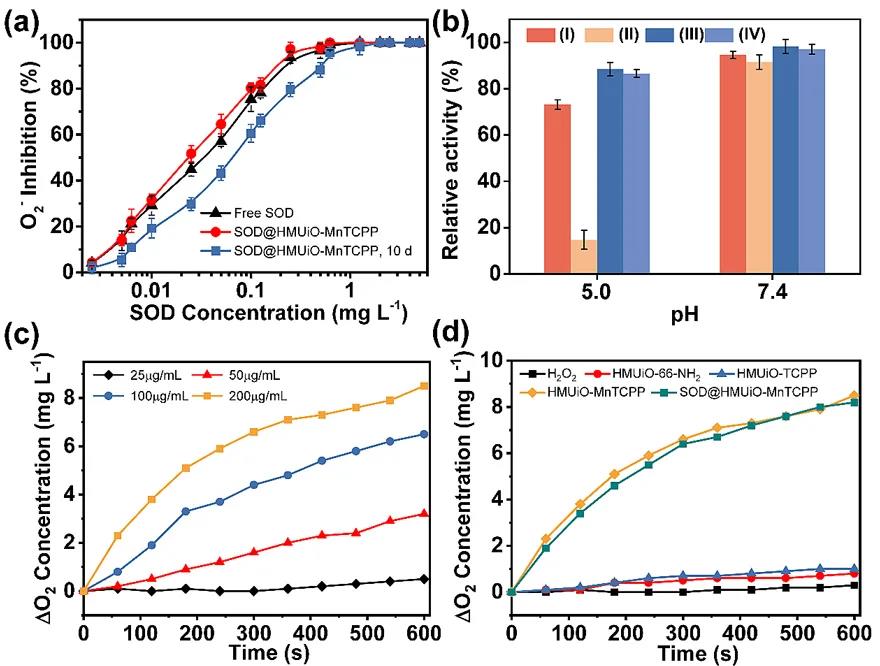
ļS║¾Ż¼įōłFĻĀ▓╔ė├░┘▓▌┐▌Ż©PQŻ®ū„×ķč§╗»æ¬╝żį┤üĒ┤╠╝żHeLa╝Ü░¹ā╚ROSĄ─▀^▒Ē▀_Ż¼ęį┤╦×ķ─Żą═Öz£yįō┐╣č§╗»ŽĄĮyī”╝Ü░¹Ą─▒Żūo─▄┴”ĪŻ╚ńłD5a║═5b╦∙╩ŠŻ¼SOD@HMUiO-MnTCPPī”╝Ü░¹╗Ņ┴”Ą─ė░Ēæ┼cä®┴┐│╩š²ŽÓĻPĪŻ═¼ĢrŻ¼┼c╬┤╠Ä└Ē╝Ü░¹ŽÓ▒╚Ż¼HMUiO-MnTCPP║═ė╬ļxSOD╠Ä└ĒĮMĄ─╝Ü░¹┤µ╗Ņ┬╩āH┬įėąį÷╝ėĪŻ▒Ē├„┴╦SOD@HMUiO-MnTCPPųą╠ņ╚╗SOD║═─ŻöMCAT├Ėī”ROSŪÕ│²Ą─ģf═¼ū„ė├Ż¼╩╣įō╝{├ūŽĄĮyŠ▀ėąĖ³’@ų°Ą─┐╣č§╗»▒Żūo╦«ŲĮĪŻ×ķ▀Mę╗▓Į▒O£y▓╗═¼MOFs╠Ä└Ē║¾╝Ü░¹ųąROSĄ─║¼┴┐Ż¼▓╔ė├2Ī»Ż¼7Ī»-Č■┬╚¤╔╣Ō╦žČ■ęę╦߯©DCFH-DAŻ®Ę©▀Mąą£yįćĪŻĮøPQŅA╠Ä└Ē▀^Ą─HeLa╝Ü░¹┐╔į┌╝ż╣Ō╣▓Į╣Æ▀├Ķ’@╬óńRŻ©CLSMŻ®│╔Ž±ųą«a╔·’@ų°¤╔╣Ōį÷ÅŖŻ¼┼c╝Ü░¹ā╚Ė▀╦«ŲĮĄ─ROSŽÓī”æ¬Ż©łD5cŻ®ĪŻČ°ĮøSOD@HMUiO-MnTCPPŅA╠Ä└Ē▀^Ą─╝Ü░¹ā╚¤╔╣Ō├„’@£p╚§Ż¼▀Mę╗▓ĮūC├„įōŽĄĮyī”ROS═╗│÷Ą─ŪÕ│²─▄┴”ĪŻ┤╦═ŌŻ¼ę“č§╗»æ¬╝ż«a╔·Ą─p-p38║═COX-II▒╗▀xū„╔·╬’ś╦ėø╬’▀Mę╗▓Įįuārįō╝{├ū¾wŽĄĄ─┐╣č§╗»─▄┴”ĪŻWestern BlotĮY╣¹▒Ē├„Ż¼į┌SOD@HMUiO-MnTCPPų╬»¤ĮMųąŻ¼╝Ü░¹ā╚p-p38║═COX IIĄ─▒Ē▀_╦«ŲĮ’@ų°£p╔┘Ż¼į┘┤╬šf├„╦∙įOėŗ║Ž│╔Ą─╣”─▄╗»╔·╬’Ę┤æ¬Ų„Š▀ėąŪÕ│²╝Ü░¹ā╚O2-║═H2O2Ą──▄┴”Ż¼─▄ėąą¦Ąž▒Żūo╝Ü░¹├Ō╩▄č§╗»ōpé¹Ż©łD5dŻ®ĪŻ
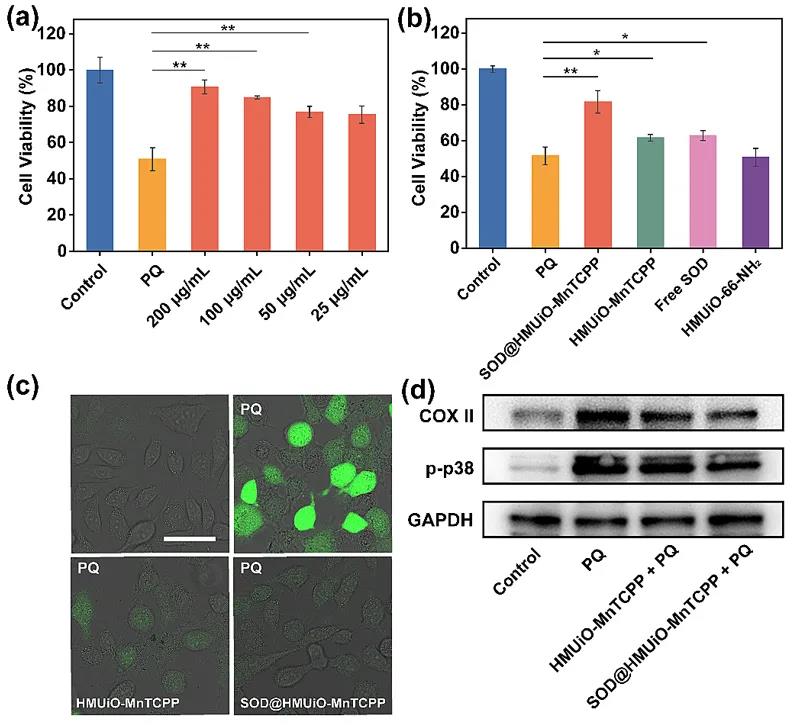
ŽÓĻPšō╬─░l▒Ēį┌Chemistry of Materials╔ŽŻ¼╚A¢|└Ē╣ż┤¾īW▓®╩┐蹊┐╔·└Ņ┐╔×ķ╬─š┬Ą─Ą┌ę╗ū„š▀Ż¼ŅÖĮśŪĮ╠╩┌×ķ═©ėŹū„š▀ĪŻ
| £ž▄░╠ß╩ŠŻ║╠Kų▌▒▒┐Ų╝{├ū╣®æ¬«aŲĘāHė├ė┌┐Ų蹯¼▓╗─▄ė├ė┌╚╦¾w,▓╗═¼┼·┤╬«aŲĘęÄĖ±ąį─▄ėą▓Ņ«ÉĪŻŠWšŠ▓┐Ęų╬─½I░Ė└²łDŲ¼į┤ūį╗ź┬ōŠWŻ¼łDŲ¼āH╣®ģó┐╝Ż¼šłęįīŹ╬’×ķų„Ż¼╚ńėąŪųÖÓšł┬ōŽĄ╬ęéā┴ó╝┤äh│²ĪŻ |
╔Žę╗Ų¬Ż║ ╬„░▓Į╗┤¾╠ŲŠ┤▀_/╣■ʵiųŠäéĪČMatterĪĘ:
Ž┬ę╗Ų¬Ż║ ╝{├ūßtīW«aŲĘ1


